新品上线 | μCaler® 甲基化检测助力实现多癌种早筛新突破 (下)
在上篇中 (新品上线 |
μCaler® 甲基化检测助力实现多癌种早筛新突破 (上)),我们全面介绍了当前癌症早筛检测的现状,并简单介绍了即将推出的纳昂达 μCaler® 靶向甲基化测序解决方案。这一全流程方案具有多项鲜明的特色,包括精准检测大规模 CpG 位点、精确定量不同甲基化状态样本的甲基化水平、高速便捷操作、稳定高效捕获、更低的测序成本以及稳定的交付周期。
μCaler® 靶向甲基化测序解决方案是纳昂达全球独创的具有自主知识产权的创新性方案,其搭载了独家专利的 μCaler® 杂交捕获系统,旨在为用户提供全新的甲基化测序体验,确保精准、稳定、高效、快速、简单。在本期内容中,我们将通过性能表现数据和真实样本应用示例,为大家展示 μCaler® 靶向甲基化测序解决方案的卓越性能。
01 μCaler® 靶向甲基化测序解决方案
1.1 方案特色
• 精准检测大规模 CpG 位点:一次性检测多种癌症的多个基因的 CpG 位点,实现精准联合检测;
• 精确定量甲基化水平:高精度覆盖 0-100% 不同甲基化状态样本的精准定量;
• 高速便捷操作:实验流程简化,操作便捷,单日内完成全部流程;
• 稳定高效捕获:避免数据量不一致,确保捕获测序结果的稳定性,降低返工风险;
• 更低检测成本:采用混杂模式,减少杂交捕获数量,降低测序成本,提升经济效益。
1.2 μCaler® 甲基化探针设计特点
μCaler® 靶向甲基化测序解决方案采用先转化后捕获的实验流程,其甲基化探针基于转化后的 DNA 模板链采用穷尽法设计思路,针对不同甲基化状态的靶标实现全面覆盖,主要有如下特点:
• 多探针快速寻找靶标形成稳定结合,以高效捕获靶标;
• 多探针间共轭效应去除非特异性结合的同时减少靶标的损失;
• 探针分别捕获甲基化和未甲基化状态的双链 DNA 信息。
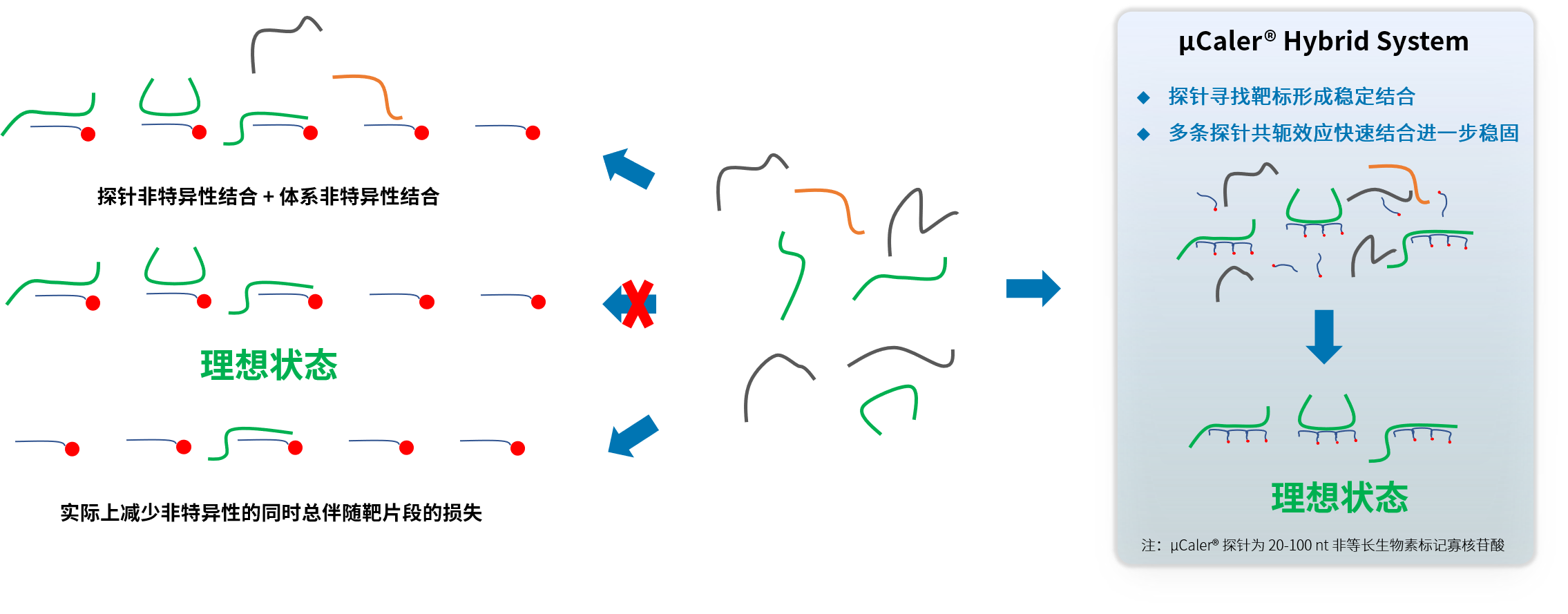
图 1. μCaler® 探针设计策略。
02 方案表现
2.1 精准检测大规模 CpG 位点
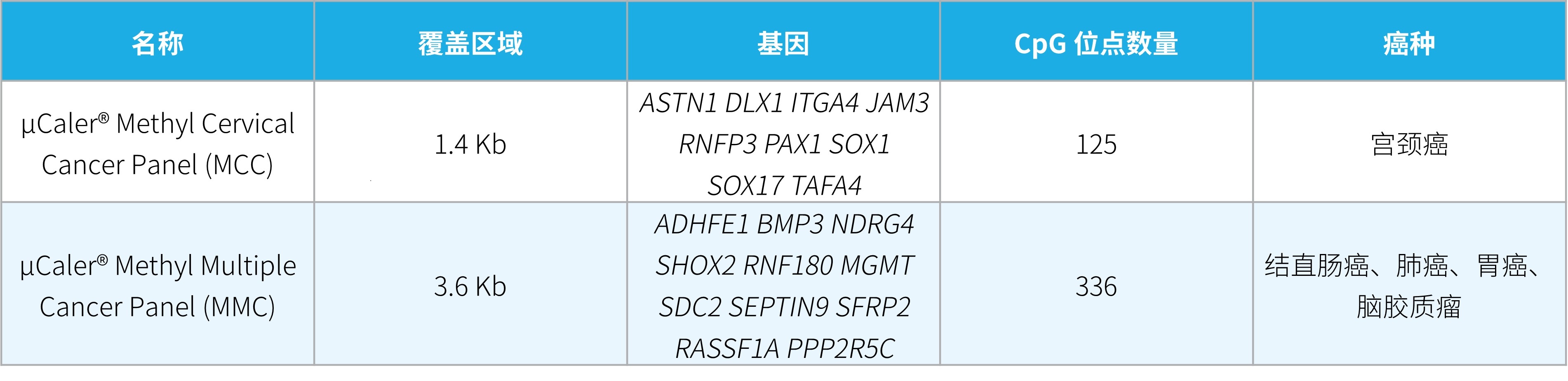
我们选取了 NMPA 获批的甲基化检测试剂盒以及文献报道中相关的甲基化标志物设计了两款含有不同规模 CpG 位点的定制 Panel,具体信息如下表:
表 1. 定制 Panel 基本信息。
人类基因组 DNA 标准品 (Promega, G1471) 利用 NadPrep® Methyl Library Preparation
Module 搭配 NadPrep® Methyl Stubby Adapter (UDI) Module
(with 10 nt Index) 和 NadPrep® DNA Methyl Bisulfite
Conversion Module 构建预文库,以 MCC 和 MMC 完成杂交捕获。结果显示,μCaler® 靶向甲基化测序方案针对不同规模的 CpG 位点均能够全面覆盖且重复再现性也非常稳定;此外,捕获数据的中靶率稳定维持在 40% 以上,0.2x mean CpG 覆盖度也达到了 99% 以上。该方案提供了高灵活性的定制选择,使用户能够根据研究需求选择不同的定制 Panel 或进行无限制性拓展,以满足特定的甲基化位点检测要求。
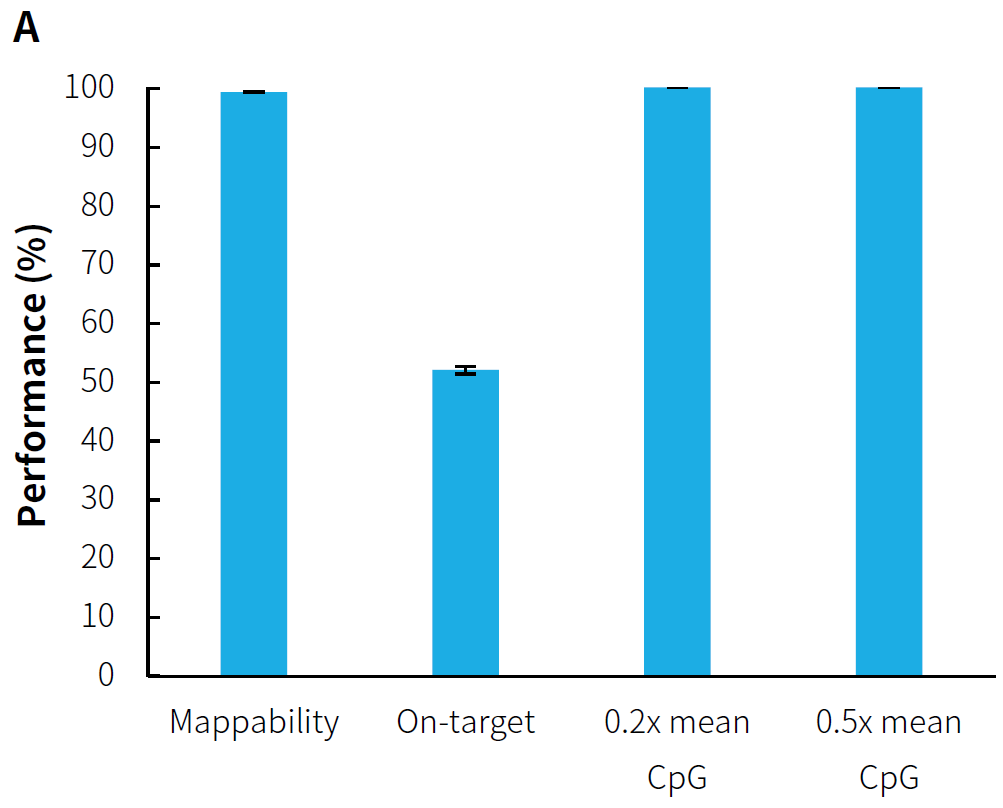
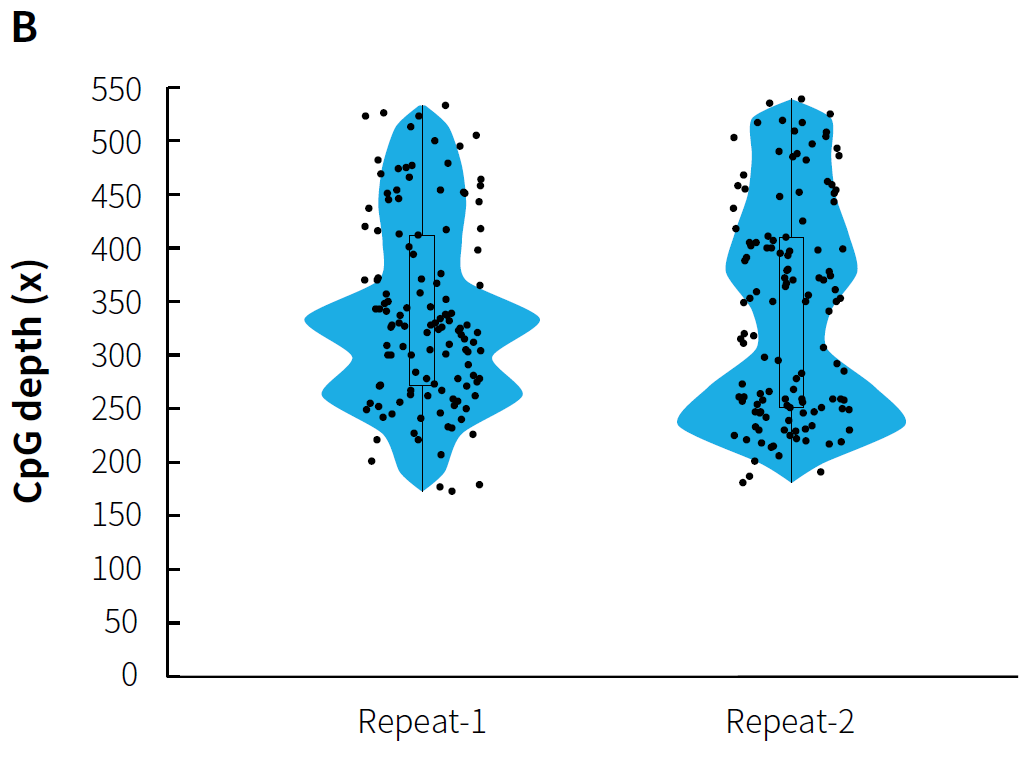
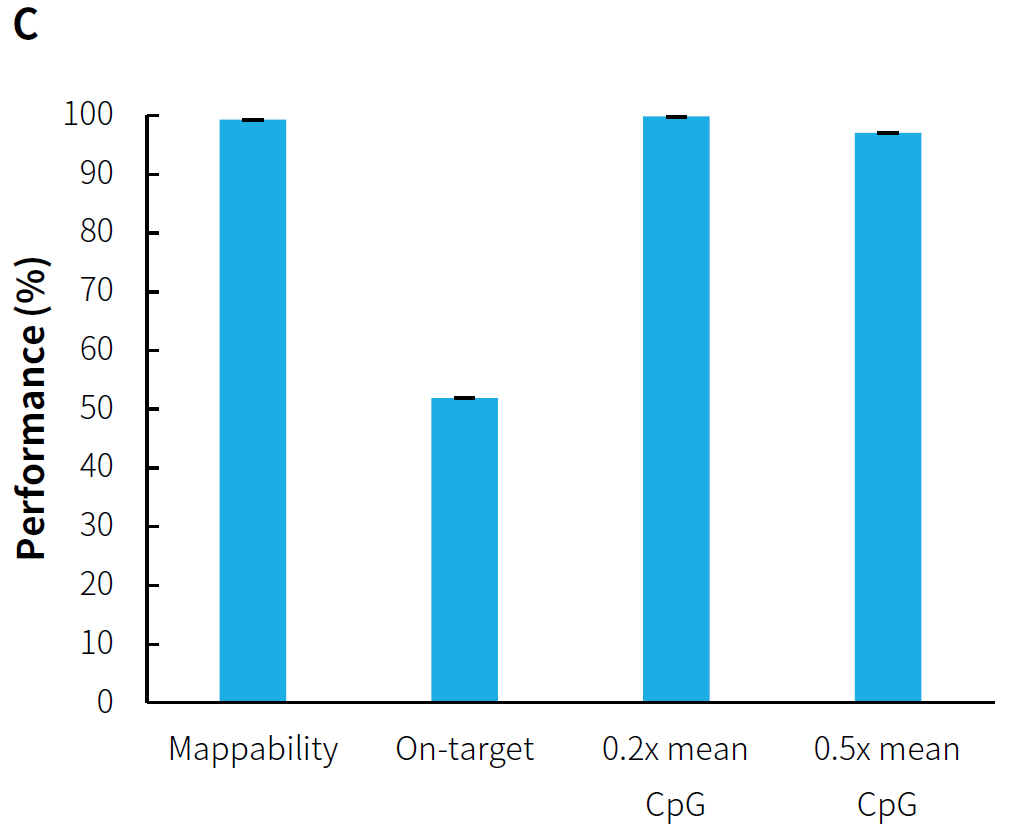
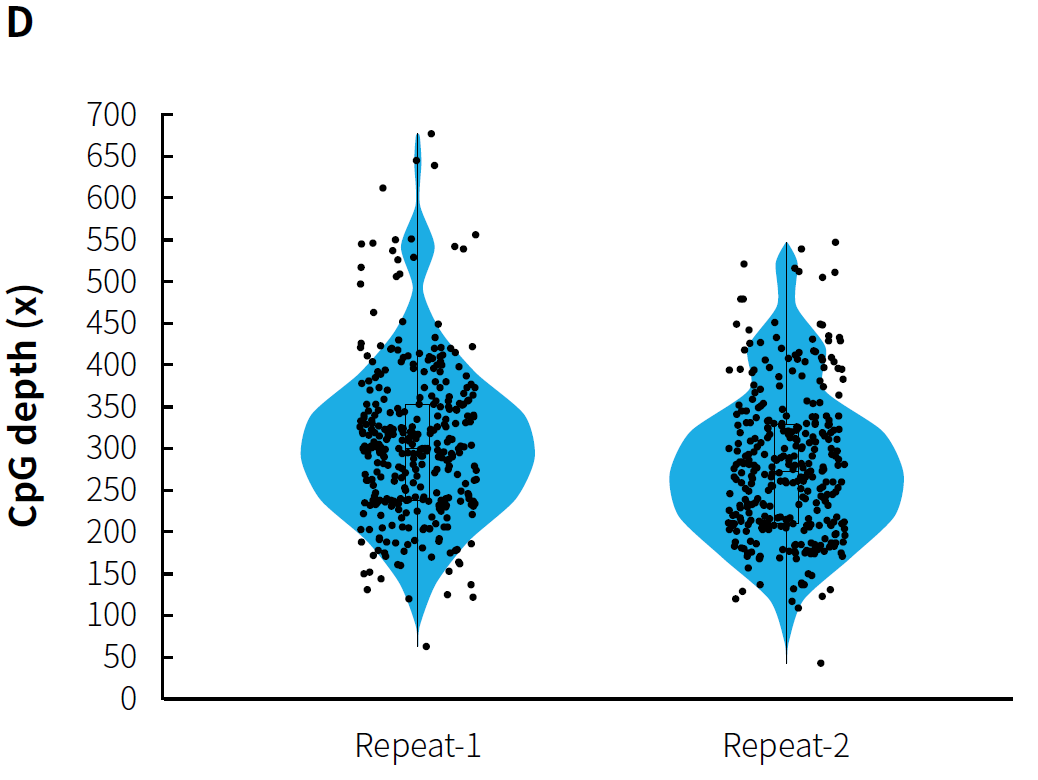
图 2. 含不同规模 CpG 位点的定制 Panel 的 μCaler® 靶向甲基化测序表现。A. MCC 捕获表现;B. MCC CpG 位点的覆盖深度;C. MMC 捕获表现;D. MMC CpG 位点的覆盖深度。
注:Illumina® Novaseq 6000,PE 150 测序,每个样本随机选取 1 Mb reads pair 用于数据分析。
2.2 精准定量甲基化水平
将 μCaler® 靶向甲基化测序方案应用于不同甲基化水平 (0%、10%、50% 和 100%) 的模拟样本,结果显示该方案在所有测试样本中均能实现较高的覆盖深度且均一性良好 (图 3.A)。此外,μCaler® 靶向甲基化测序方案的甲基化水平检测结果与理论水平高度一致 (图 3.B),表明该方案具有可靠的准确性和可重复性。这些结果均表明,μCaler® 靶向甲基化测序方案是一种高效、可靠的甲基化检测技术,适用于各种甲基化水平的研究样本。
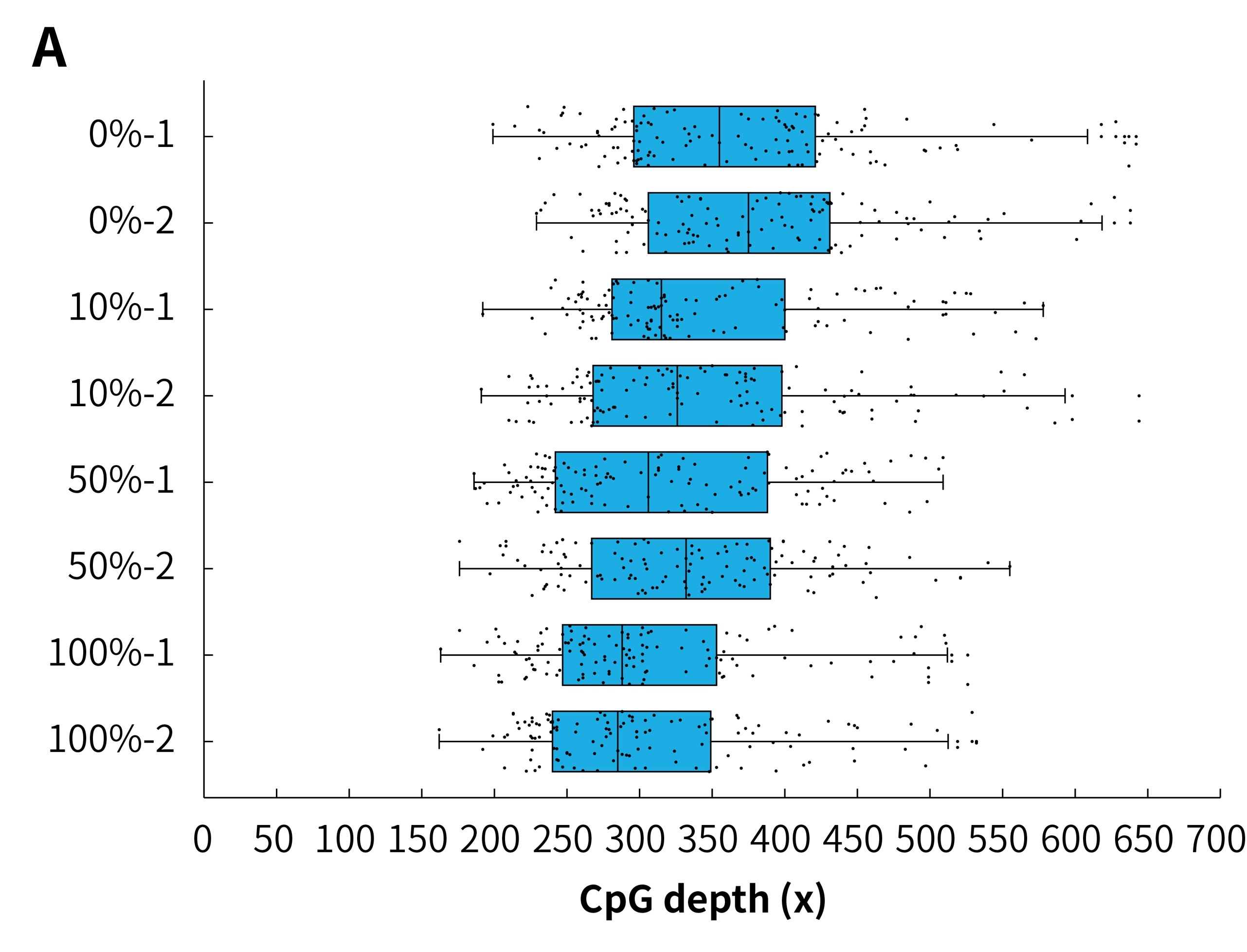
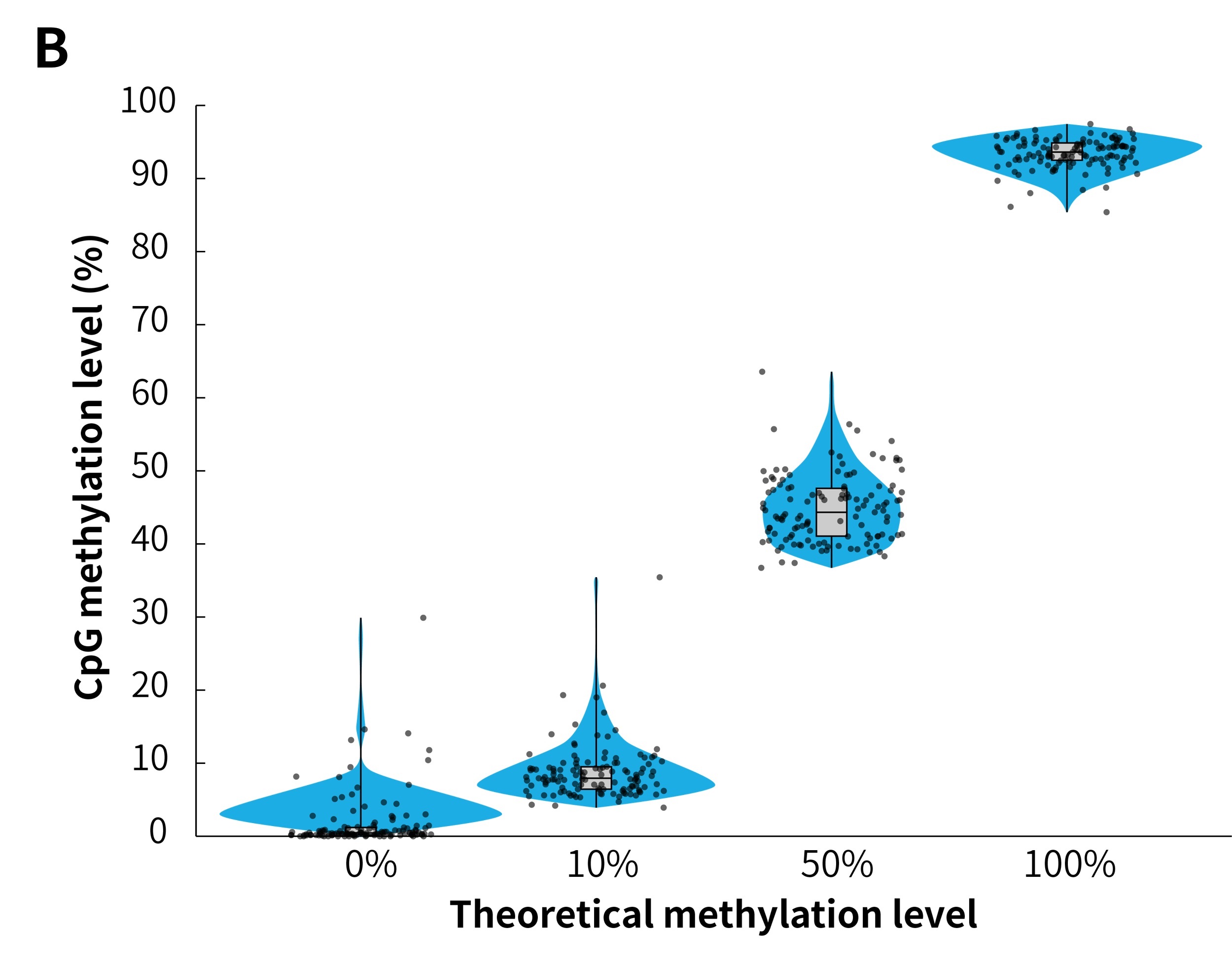
图 3. 不同甲基化水平样本使用 μCaler® 靶向甲基化测序表现。A. 不同甲基化水平样本的 CpG 位点的覆盖深度;B. 样本理论甲基化水平与使用μCaler® 靶向甲基化测序结果对比。
2.3 高速便捷操作
传统杂交捕获的痛点在于较长的杂交反应耗时以及复杂繁琐的实验操作流程,而 μCaler® 杂交捕获系统的出现不仅简化了杂交捕获的实验流程,还进一步缩短了反应的时长。从图 4. 中可以明显看出,μCaler® 杂交捕获系统的全流程平均耗时仅需 4 小时,实现了高速便捷的操作。这不仅使实验更加迅速,同时也提升了实验室的工作效率,为研究人员提供了更为便利的条件,使得杂交捕获技术在实际应用中更具吸引力。
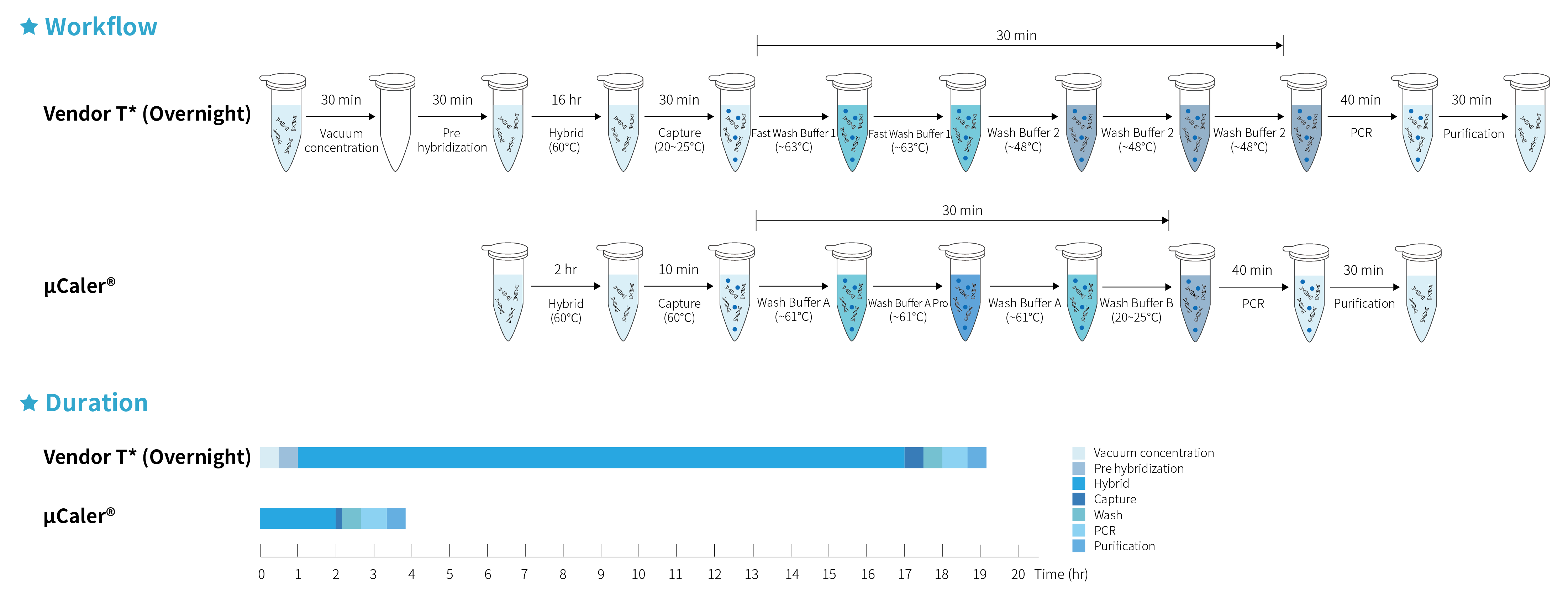
图 4. 传统杂交与 μCaler® 杂交捕获实验流程及耗时对比。
2.4 稳定高效捕获
μCaler® 甲基化杂交捕获体系经过对 AT-rich 等特殊区域的优化,与三款定制 mini Panel 搭配使用,依然展现了出色的捕获表现,保持了较高的稳定重现性。这种优化设计使 μCaler® 甲基化杂交捕获体系与不同的 mini Panel 相适应,为用户提供了更灵活、可定制的选择,以满足不同研究需求。
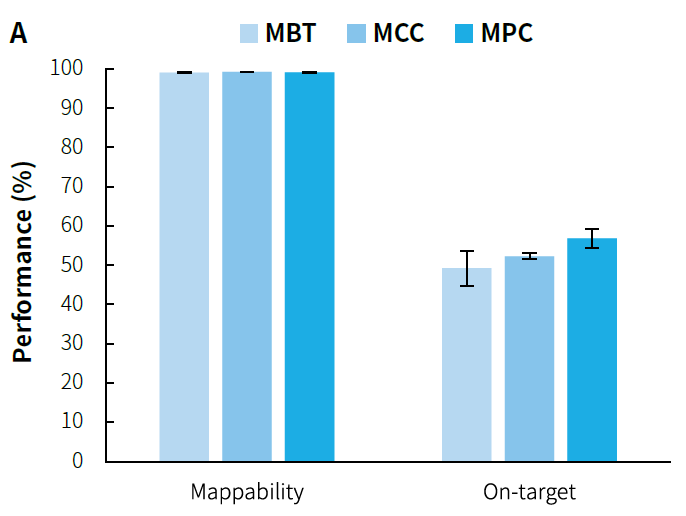
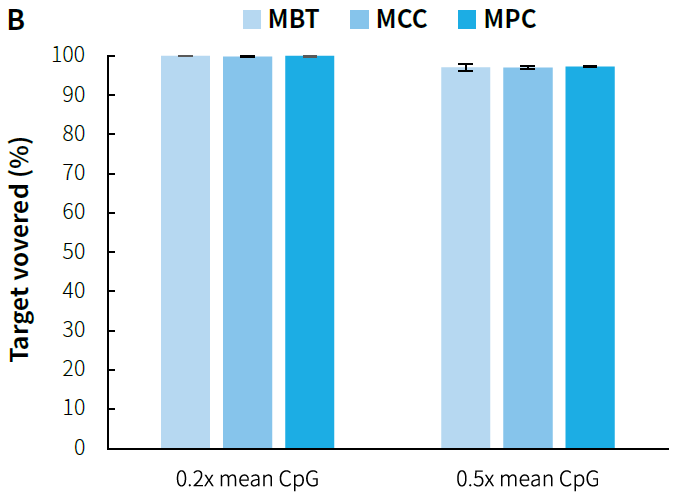
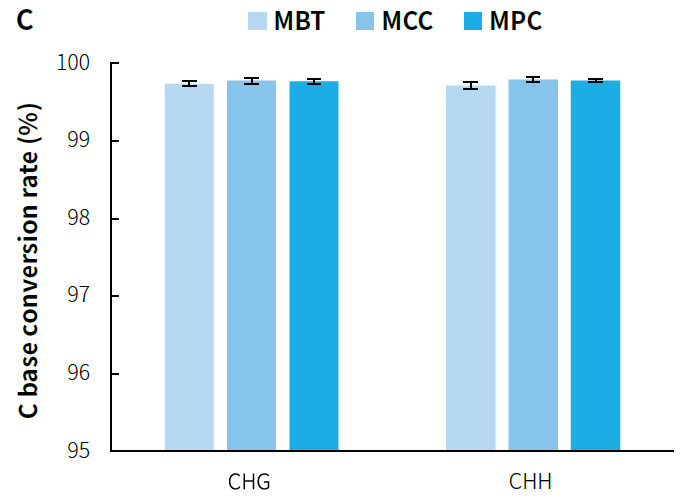
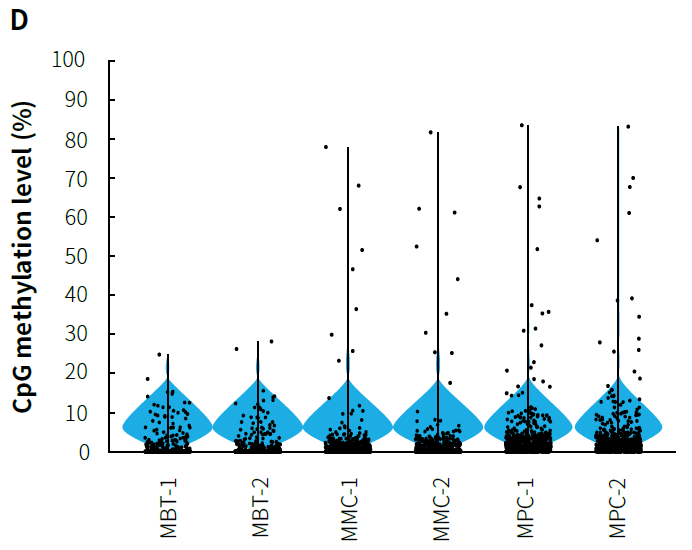
图 5. μCaler® 靶向甲基化测序对小 Panel 的捕获表现。利用人类基因组 DNA 标准品 (Promega, G1471) 构建预文库,500 ng/ 预文库投入,分别以 MBT、MMC 和 MPC 完成杂交捕获。A. 捕获数据的比对率和中靶率;B. 靶区域 CpG 位点覆盖度;C. C 碱基的转化率;D. CpG 位点的甲基化水平。
注:MBT 覆盖区域约 1.2 Kb,包含 159 个 CpG 位点;MPC 覆盖区域约 6.2 Kb,包含 620 个 CpG 位点。
2.5 更低检测成本
靶向甲基化测序成本高,通过建立多样本混合杂交方案有效降低试剂和人力成本,显著提高实验效率。如图 6. 所示,与单文库杂交相比,采用 6 个文库混合杂交的 μCaler® 系统在降低实验成本的同时,仍能保持数据质量,并实现更高的性价比。
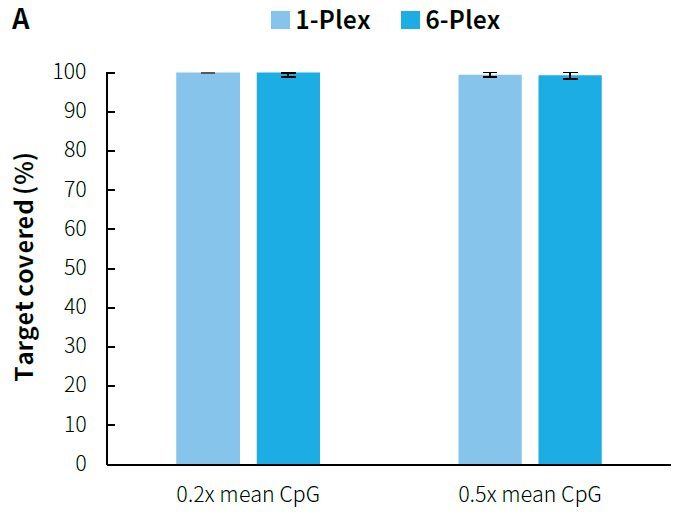
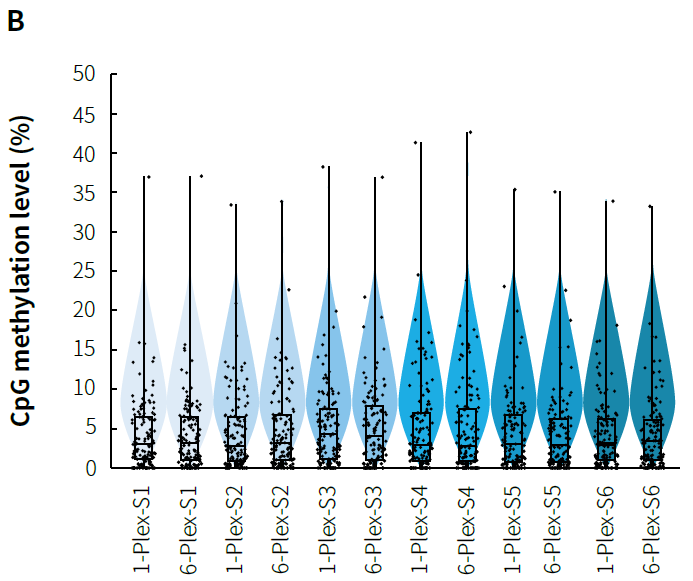
图 6. 不同混合杂交方式下的 μCaler® 靶向甲基化测序的捕获表现。利用人类基因组 DNA 标准品 (Promega, G1471) 构建预文库,500 ng/ 预文库投入,以 MCC 完成杂交捕获。A. 靶区域 CpG 位点覆盖度;B. CpG 位点的甲基化水平。
03 临床真实样本应用示例
癌症早筛队列研究选取多种技术路线,旨在对全基因组筛选的甲基化 Biomarker 进行验证,尽可能满足高灵敏度、覆盖范围广且成本可控等多种需求。研究人员分别采用 μCaler® 靶向甲基化测序 (μCaler) 和多重 PCR 扩增 (Amp) 对两例不同甲基化水平的临床 gDNA 样本 (Tumor:甲基化水平相对高;Normal:甲基化水平相对低) 进行了 CpG 位点的甲基化水平检测。图 7. 显示,两种技术针对不同甲基化状态样本的检测结果存在差异,μCaler 适用于不同甲基化状态的样本检测,Amp 对于不同甲基化状态的靶标具有一定的偏好性,部分区域无法覆盖。以 7 号染色体 (Chr 7) 相关 CpG 位点的检测结果进一步展示,采用 Amp 对于高甲基化状态样本检测到的甲基化水平低于 μCaler,而对于低甲基化状态样本的检测结果为 N。


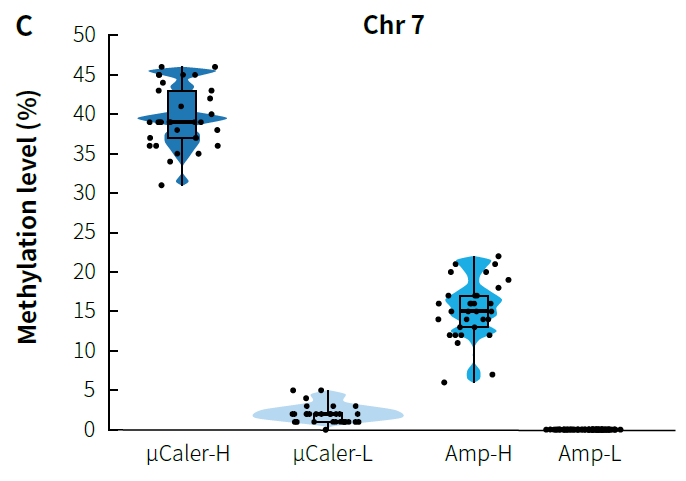
图 7. 不同技术路线对临床真实样本的检测结果比较。A. 高甲基化水平样本 (Tumor) 的检测结果; B.低甲基化水平样本 (Normal) 的检测结果;C. 7 号染色体 (Chr 7) 相关 CpG 位点甲基化水平。
注:μCaler® 靶向甲基化测序以 MBT 完成杂交捕获。
究其原因,主要有以下几点:1) 多重 PCR 扩增引物设计复杂度高,对于不同甲基化状态的区域,扩增具有一定的偏好性;2) GC-rich 区域转化后会成为 AT-rich 或者 GC-rich 区域,PCR 扩增难度较大,会出现部分区域覆盖较差甚至没有覆盖的情况;3) 设计甲基化多重引物时,引物结合位点不能包含 CpG 位点,对于连续 CpG 区域无法设计引物。
此外,在 20 例临床真实样本的检测中,μCaler® 杂交捕获体系依然表现出稳定的捕获性能。如图 8. 所示。
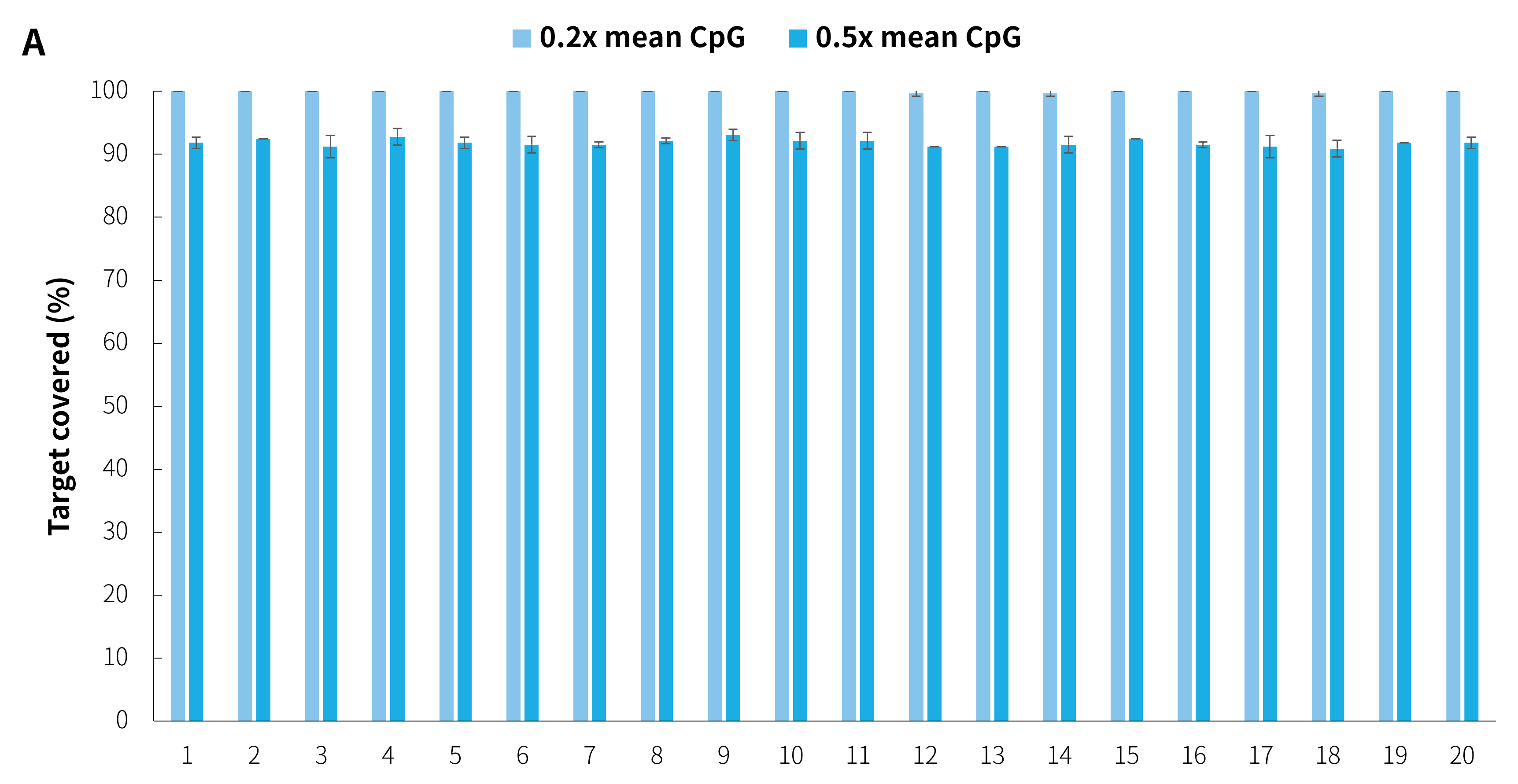

图 8. μCaler® 靶向甲基化测序对临床真实样本的捕获表现。A.靶区域 CpG 位点覆盖度;B. CpG 位点的甲基化水平。
综上所述,相较于多重 PCR 扩增技术,μCaler® 靶向甲基化测序解决方案在临床真实样本的检测中表现出更高的检测灵敏度以及稳定性。
04 应用展望
肿瘤早筛行业呈现差异化竞争格局,其中单癌种的筛查主要依赖 PCR 技术,而多癌种的筛查则主要采用 NGS 技术,且其具有相对较高的技术壁垒。在这一背景下,纳昂达能够为用户免费提供探针在线设计平台,用户可根据个性化需求灵活设计探针,提供定制化产品方案。其中,μCaler® 杂交捕获技术不仅具备自主知识产权保护,还为产品的顺利落地提供了坚实的保障,为客户在肿瘤早筛领域的发展保驾护航。
早筛产品的临床研究主要分为回顾性和前瞻性两种。纳昂达专注于为临床队列研究提供全流程解决方案和技术支持,包括甲基化位点筛选、验证和早筛产品开发。全面的技术解决方案将有助于加速早筛产品的研究进程,为肿瘤早期诊断领域做出贡献。








