μCaler® RIA Solution 解锁呼吸道感染精准诊疗新范式
在上篇中,我们围绕呼吸道感染诊疗面临的核心挑战,重点探讨了从 “经验用药” 向 “精准诊疗” 转变的必然趋势,并系统介绍了 μCaler® RIA Solution 在多病原体检测、耐药特征解析及结果解读方面的整体设计思路。
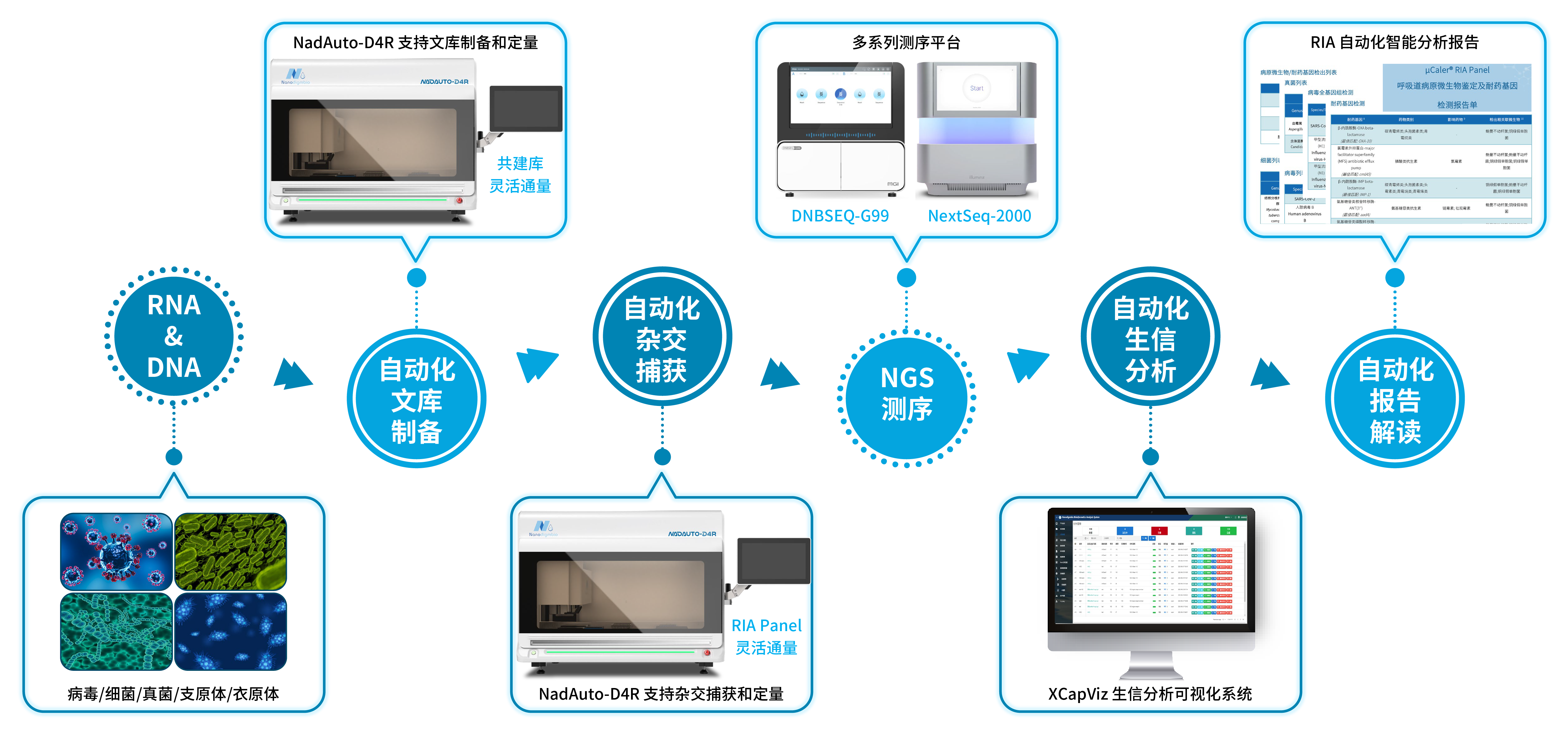
图 1. μCaler® RIA Solution 一体化解决方案。
在此基础上,我们进一步认识到,在实际临床应用中,呼吸道感染诊疗中更为关键的问题在于:检测能力的提升,是否能够真正转化为临床价值?换言之,一套检测方案不仅需要“看得见病原”,更应能够辅助临床判断、指导用药,并在复杂感染场景中提供可落地的决策依据。因此,评价一套方案的核心,不仅在于其技术性能,更在于其在真实临床环境中的应用表现及其对临床决策的支持能力。那么,μCaler® RIA Solution 在呼吸道感染检测场景中的实际表现如何?本篇将从检测性能与耐药解析能力等方面进行进一步阐述。
01 稳定检出标准品中多病原体
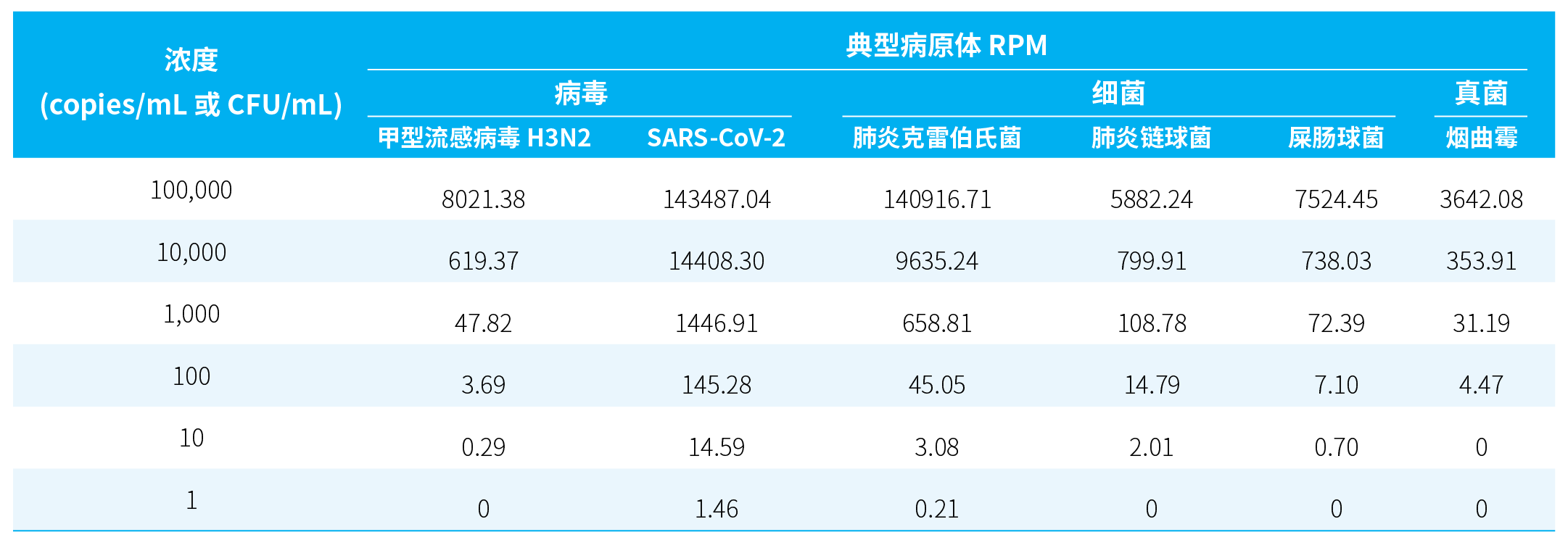
为系统评估 μCaler® RIA Solution 在呼吸道感染检测场景中的性能表现,我们对微生物标准品进行了梯度稀释,分析其在不同浓度条件下对代表性病原体 (甲型流感病毒 H3N2、SARS-CoV-2、肺炎克雷伯氏菌、肺炎链球菌、屎肠球菌、烟曲霉) 的检出能力。具体而言,分别取 0.4 mL 不同浓度梯度的标准品,提取 RNA & DNA 混合核酸,利用 NadPrep® 快速 RNA & DNA 共建库试剂盒进行预文库构建,以 μCaler® 超级预混杂交捕获试剂盒 (Illumina 平台) 和 μCaler® RIA Panel v1.0 完成杂交捕获。RPM 分析结果显示,在所评估的 3 类共 6 种病原体中,除烟曲霉外,其余病原体均可在低至 10-100 copies/mL 或 10-100 CFU/mL 的条件下实现稳定检出。值得强调的是,得益于 μCaler® RIA Panel 对 SARS-CoV-2 的全基因组覆盖设计,μCaler® RIA Solution 对其检测灵敏度可低至 1-10 个基因组拷贝数 (表 1)。
表 1. μCaler® RIA Solution 对标准品中多病原体的检测限。
此外,我们进一步评估了 μCaler® RIA Solution 在标准品中对多种病原体进行批内及批间检测的稳定性。基于 RPM 分析结果显示,该方案对标准品中涵盖的多类型病原体 (包括病毒、细菌和真菌) 在不同批次间均可实现稳定检出,且同一批次内各重复样本之间的检测结果具有良好一致性 (图 2)。结果表明,μCaler® RIA Solution 在多病原体检测场景下具备优异的重复性与可靠性,可满足临床高通量与高稳定性检测的应用需求。
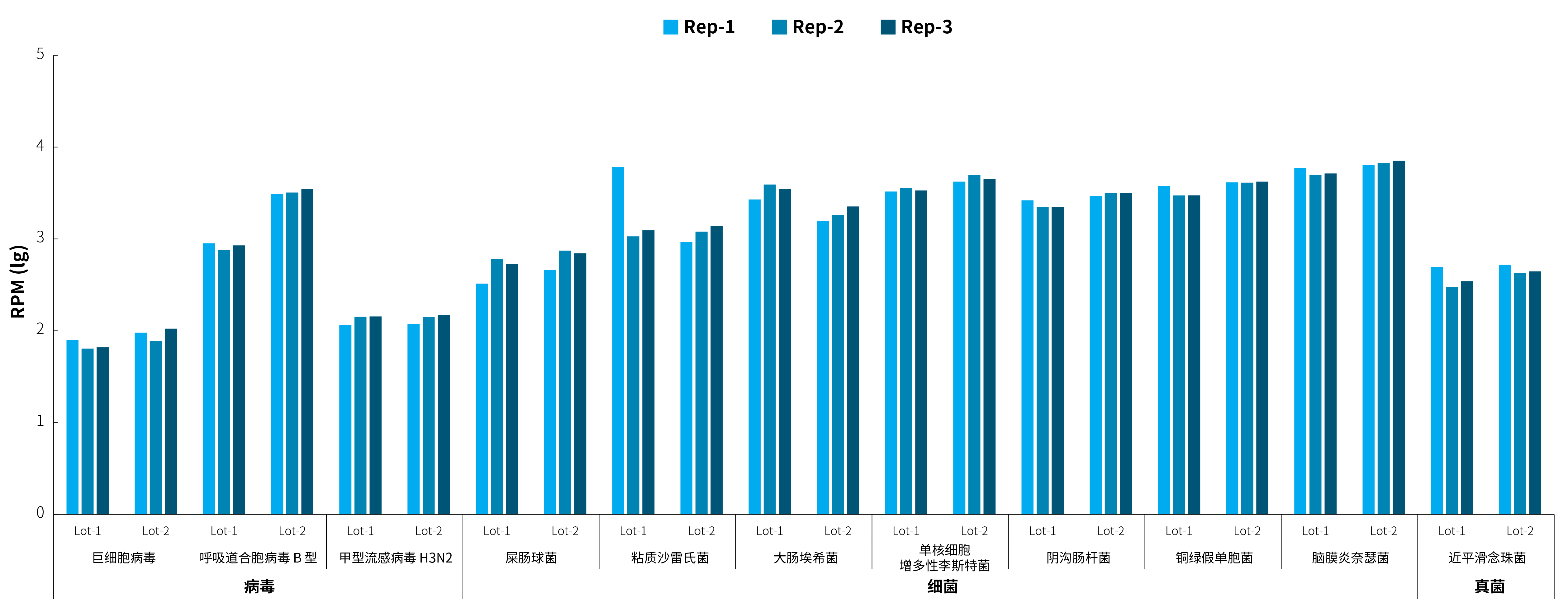
图 2. μCaler® RIA Solution 对标准品中多病原体的批内及批间检测稳定性评估。
02 有效提升临床关键病原体检出率
为系统评估 μCaler® RIA Solution 与传统常规临床检测方法在 6 种重要病原体检测中的性能差异,我们对来源于 78 例临床患者 (涵盖痰液、肺泡灌洗液等多种样本类型) 的检测结果进行了整合分析。结果显示,μCaler® RIA Solution 与 mNGS 的总体检出率均显著高于传统培养法 (图 3)。其中,在耶氏肺孢子菌和诺卡菌的检测中优势尤为明显,这主要归因于上述病原体目前仍无法进行体外培养。在具体病原体层面,μCaler® RIA Solution 在结核分枝杆菌复合群 (MTBC)、耶氏肺孢子菌及烟曲霉的检出数量上高于 mNGS;而 mNGS 在非结核分枝杆菌 (NTM) 和诺卡菌的检出数量上则优于 μCaler® RIA Solution,提示两种技术在不同病原体类型上的检测优势具有一定互补性。
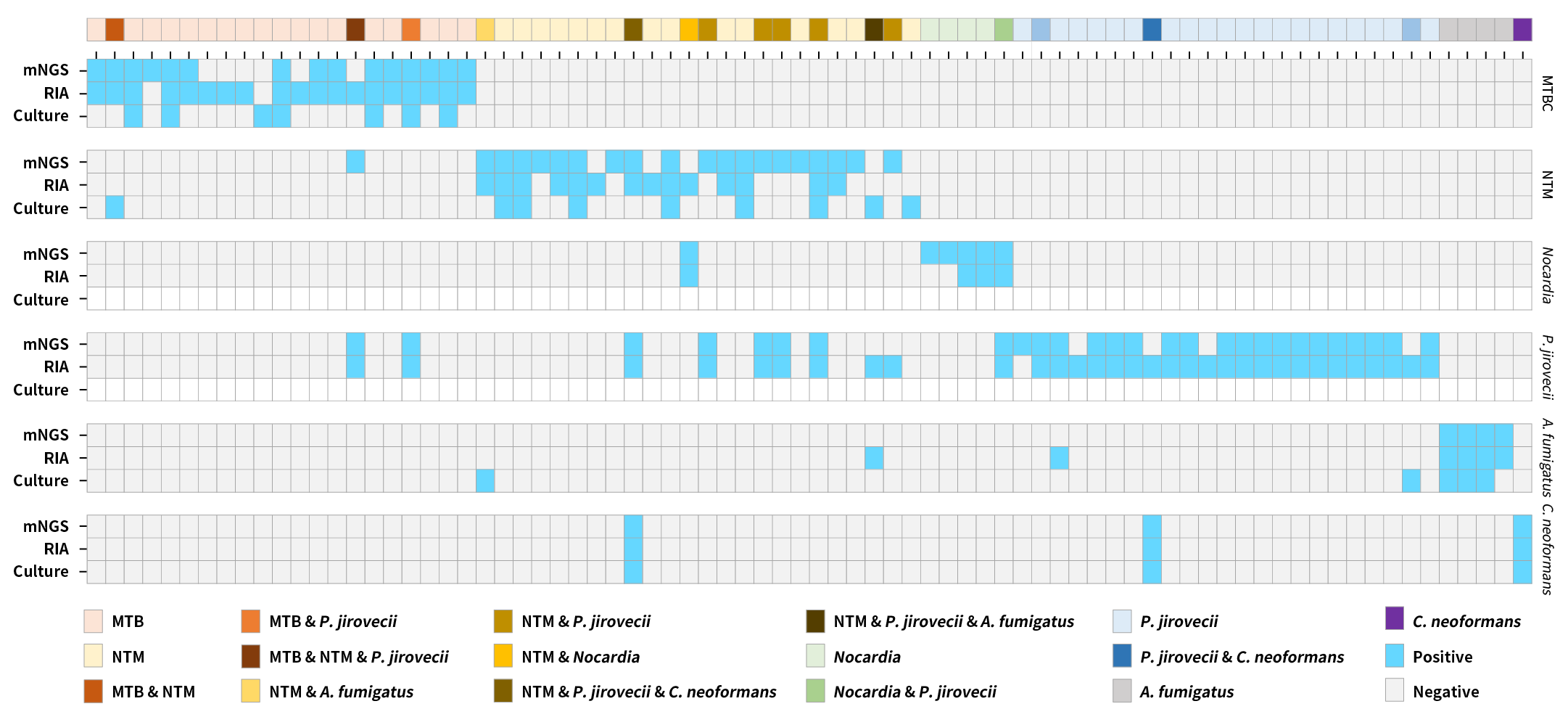
图 3. μCaler® RIA Solution、mNGS 与分离培养在临床关键病原体检出一致性的热图比较。
注:纳入分析的临床关键病原体包括:MTBC (M. tuberculosis complex, 结核分枝杆菌复合群),NTM (non-tuberculous mycobacteria, 非结核分枝杆菌;如加那利群岛分枝杆菌、堪萨斯分枝杆菌、鸟分枝杆菌、鸟-胞内分枝杆菌复合群、日内瓦分枝杆菌、龟分枝杆菌和蟾分枝杆菌等),Nocardia (诺卡菌属),P. jirovecii (耶氏肺孢子菌),A. fumigatus (烟曲霉) 和 C. neoformans (新生隐球菌)。
03 精准识别耐药基因与关联病原体
为系统评估 μCaler® RIA Solution 在耐药特征解析方面的能力,我们对其检测结果与实验室常规微生物学方法 (包括分离培养鉴定与药敏表型试验) 在 3 例临床患者中的结果进行了对比分析。结果显示,两种方法在 3 例样本中检出的病原体高度一致,分别为肺炎克雷伯氏菌、铜绿假单胞菌、鲍曼不动杆菌。此外,μCaler® RIA Solution 检测到的耐药基因,其对应的表型预测结果与药敏试验结果亦表现出高度一致性 (表 2)。由此说明,μCaler® RIA Solution 能够实现耐药基因与对应病原体的精准关联,并解析其潜在耐药药物信息,为临床用药决策提供关键分子依据,从而进一步提升呼吸道感染诊疗的临床应用价值。
表 2. μCaler® RIA Solution 对标准品中多病原体的检测限。
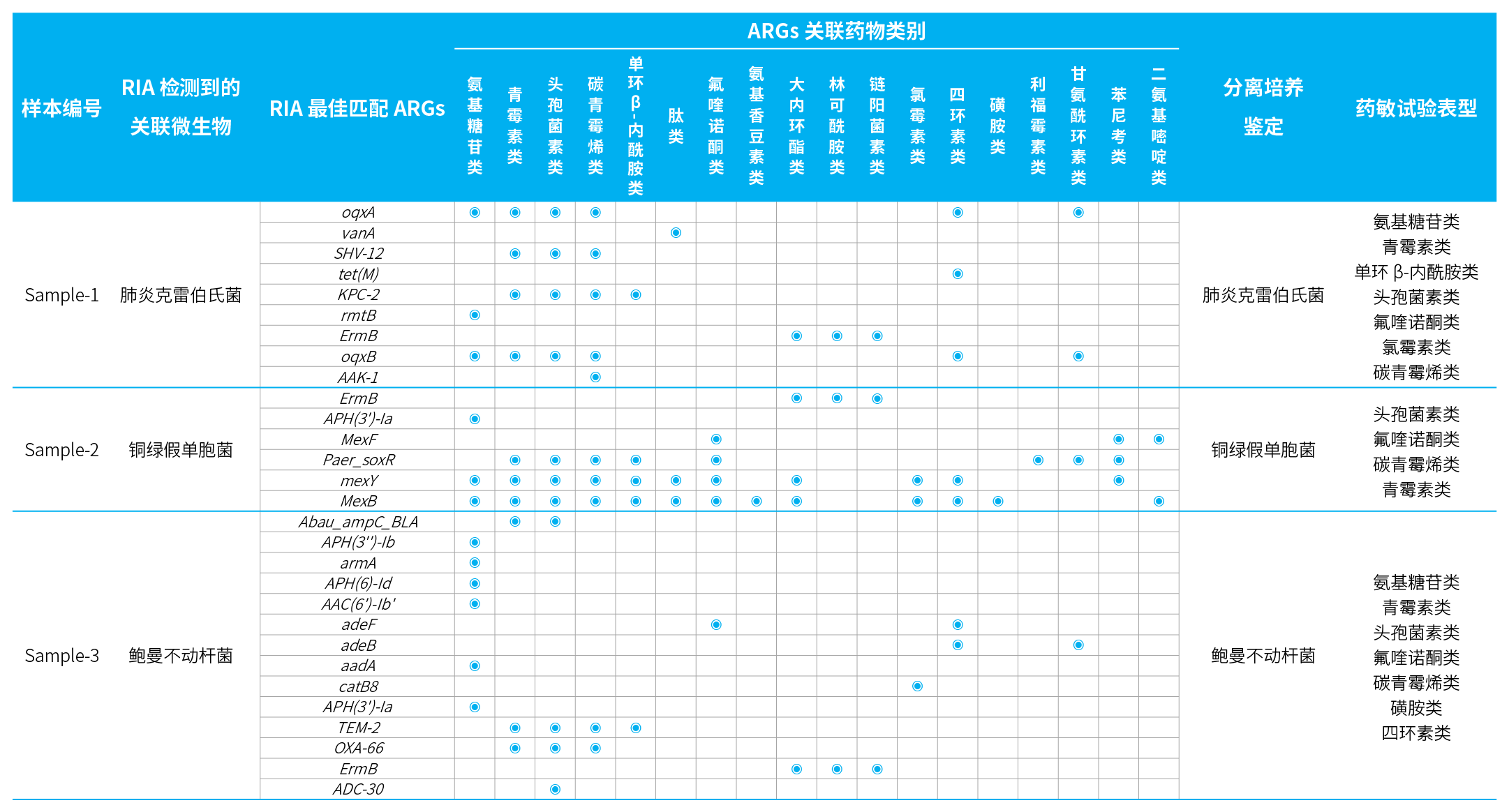
注: ARGs: Antibiotic Resistance Genes.
04 总结与展望
μCaler® RIA Solution 围绕呼吸道感染诊疗中 “检测难、解读难、决策难” 的核心痛点,构建了覆盖多病原体检测、耐药特征解析及结果智能解读的一体化解决方案。从标准品与临床真实样本的评估结果来看,μCaler® RIA Solution 在多类型病原体的检出能力、重复性与稳定性方面表现优异,能够在复杂感染场景下实现低丰度病原体的可靠识别。同时,通过对耐药基因的精准检测及其与病原体来源的关联分析,实现了分子检测结果向临床用药指导的有效转化。结合分级判读策略与多维度质量控制体系,进一步提升了检测结果的可解释性与临床参考价值。
面向未来,随着呼吸道感染病原谱的持续演变以及抗微生物药物耐药性问题的不断加剧,临床对 “快速、全面、精准且可解释” 的检测需求将愈发迫切。μCaler® RIA Solution 有望在更多临床应用场景中发挥重要作用。同时,随着算法模型与数据库的不断迭代优化,其在结果解读与临床决策支持方面的能力也将进一步增强,助力推动呼吸道感染诊疗由 “经验驱动” 向 “数据驱动” 持续升级。








